1. CRO全球市场规模达350亿美元,其中亚太地区增速最快
随着全球制药企业研发成功率降低、研发投资费用上升和药品专利悬崖的到来,目前全球已有超过50%的药企选择聘用专业CRO企业协助新药研发服务,以降低自身研发费用并控制风险。根据南方所的统计,2012年至2016年,全球CRO行业的销售额由231亿美元稳步上升至326亿美元,年复合增长率达到8.78%,呈逐年上升趋势。预计未来五年,全球CRO行业仍将持续高速增长,2021年全球CRO行业销售额将达479亿美元,年均复合增长率达8.00%
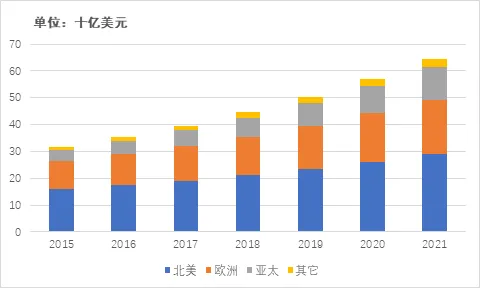
北美地区和欧洲地区仍旧占据了全球CRO市场的主要份额,其中美国CRO行业龙头昆泰占据2015年全球市场份额的16.70%。亚太地区凭借自身优势成为CRO全球市场规模增速最快的区域,预计到2021年亚太地区市场规模将达123亿美元,年复合增长率为20.3%。
图1 全球CRO行业规模及增长率(2012-2021年)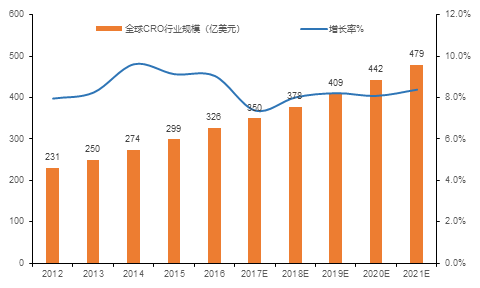
1.1 2022年全球药企研发投资费用超1810亿美元,CRO市场前景可观
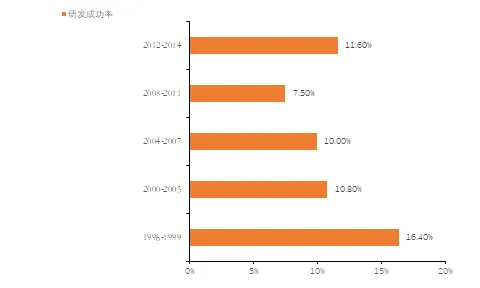
2012年全球制药行业在药品研发活动中花费了近1370亿美元,制药行业在研发活动上的费用投入约为其他高科技行业(如软件和计算机服务行业)研发投入费用的2.5倍,仅在2012年间药企通过专利合作条约(PCT)登记了7,792个专利。截止至2015年,排名前30名的药企至少与一家CRO企业展开了合作,行业龙头企业平均同时与三家CRO企业保持合作关系来维持自身的产品的合理布局。全球药企研发投入稳步增长,2022年将达到1810亿美元。全球药企新药研发的成功率逐年下降,2008-2011年期间的成功率已不足上世纪90年代后期的一半,2012-2014年期间略有回升。新药研发难度的不断提升及全球药品监管要求的不断提高都增大了药企对药品研发的投入,而这些困难均促进了药企与具备专业知识和基础设施的CRO企业达成合作。
1.2 仿药争夺“专利悬崖”时代,药企研发业务外包占比不断增大
全球医药界迎来了专利悬崖,仿制药的时代随之到来,这将对全球原研药公司造成巨大损失。据Pharma letter的报告,截至2015年底约有46项美国药品专利将到期,从2018年到2022年,专利悬崖预计将给原研药企造成82亿美元的药品销售损失。相较于新药,仿制药的研发在成本及时间上都具有显著优势,这促进了大批仿制药公司将药物开发过程外包。此外,专利到期后的药品市场竞争加剧及利润率下降都将加大大型制药公司对外包临床试验的偏好。专利悬崖促进了医药外包CRO市场的蓬勃发展。
图4 全球专利悬崖药品销售额(2008-2022年)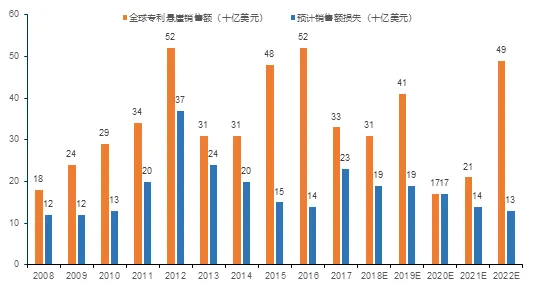
未来药企研发业务外包占比不断增大,2021年全球CRO业务渗透率有望达到46.5%。据 Frost & Sullivan预测,2016年全球药企研发费用投入为1453.8亿美元,理论上其中的1163 亿美元研发业务可以选择外包,而实际CRO市场仅为354亿美元,CRO渗透率为30.5%;预测到2021 年,CRO渗透率有望提升至46.5%。
2. CRO并购整合加速实现一站式服务,新技术纳入提升整体服务水平
2.1延伸拓展产业链,提供一站式医药外包服务,提升行业集中度
为在竞争激烈的市场中维持及增强自身优势与竞争力,医药外包企业通过并购整合不断扩张业务。2014年1月,全球领先的临床试验管理方案解决方案供应商BioClinicaI Inc.和SMO(Site management organization)公司CCBR-SYNARC签署了一项合并临床外包服务的协议,该协议将允许其为目标药企提供一系列量身定制的服务来满足客户不同的研究需求;2015年LabCorp为获得更大市场份额以55亿美元收购了Covance;2016年爱尔兰CRO企业ICON收购Clinical Research Management Inc.以扩大公司在政府资助的研究市场实力。
并购整合成为大企业快速延伸拓展产业链的手段,将分散的各阶段医药外包业务整合:①通过兼并收购补充自身业务短板;②加强与交叉领域的结合实现资源利用最大化;③同行之间收购产生协同效应不断扩大市场份额。
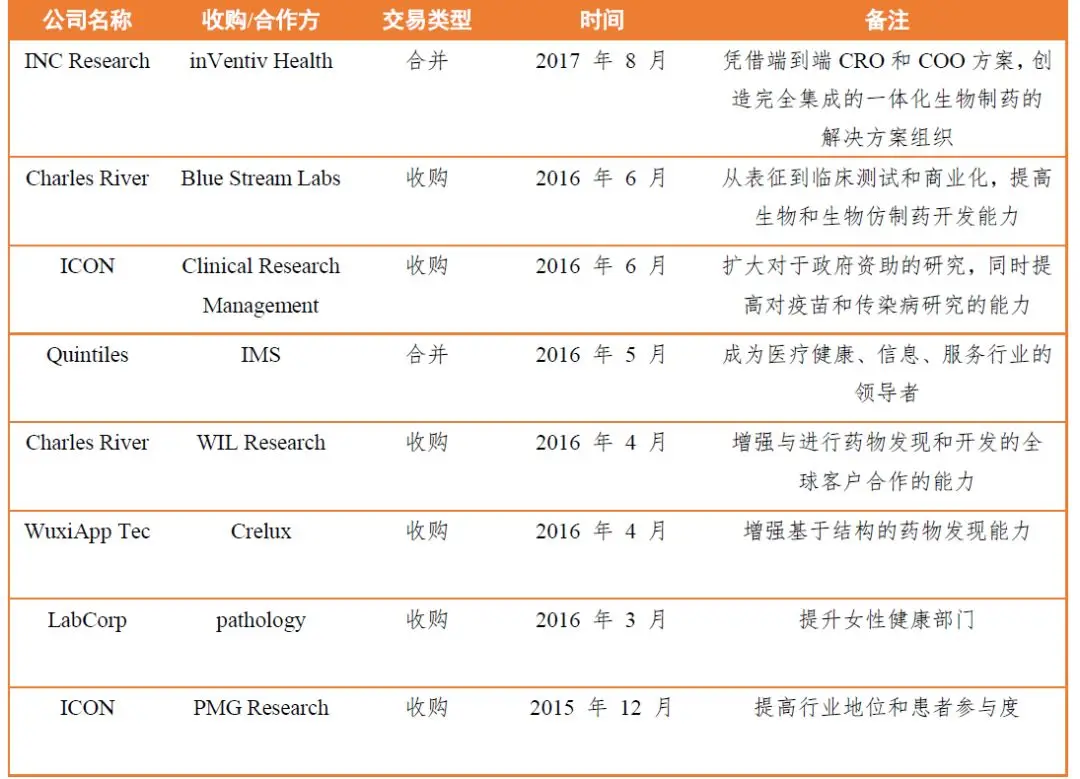
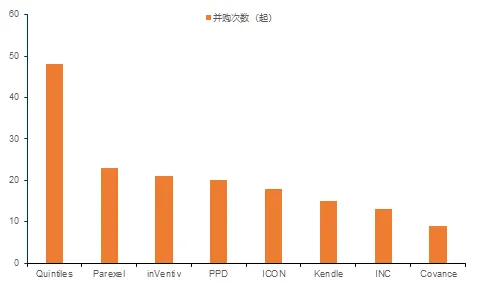
CRO行业在经历了一系列整合后,企业间差距逐渐缩小,行业竞争日趋激烈,演化出多种商业模式。大型CRO企业在发展过程中不再局限于传统的“一手交钱,一手交货”的一次性交易订单合同模式,逐渐走向“里程碑”付费的创新型模式。近年越来越多的CRO企业与药企建立“同甘共苦”的战略合作关系,商业模型转变为最前沿的结果导向型模式和风险共担模式。
表2 目前全球CRO的四种商业模式

表3 大型CRO企业近年战略合作案例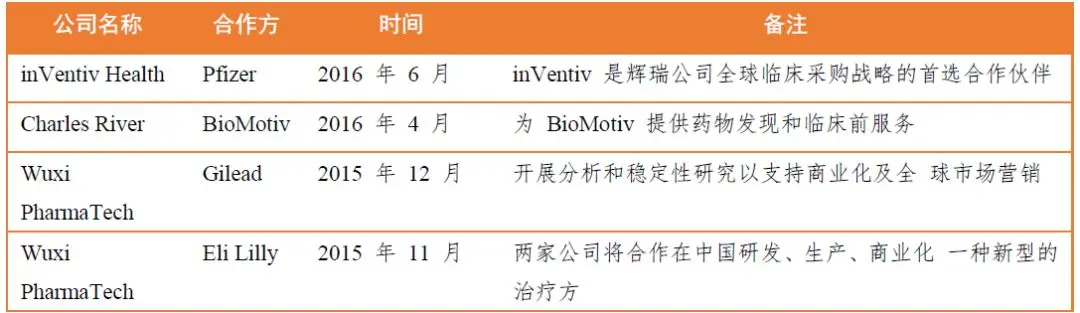
2.2 云技术的引入实现CRO与药企间的紧密合作,提高新药研发效率
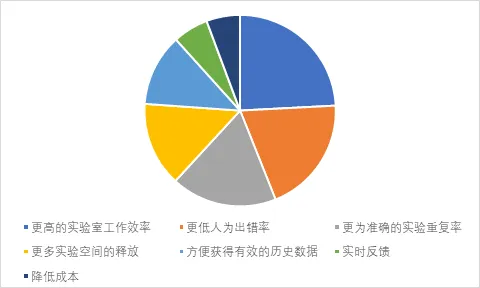
随着CRO之间竞争的加剧,引入云技术将是未来CRO的发展趋势之一,除提高CRO新药研发的效率外,方便快捷的沟通协作能够吸引进大批药企的合作,并在紧密合作中与药企建立起彼此信任的关系,有助于CRO业务的持续稳定发展。使用云技术优化数据管理系统不仅能够增加药企和CRO进行合作,还缩短了药物的研发时间。目前多数CRO企业使用的是TMF(TrialMasterFile)模式对临床试验数据进行管理,即使用纸质形式对临床数据进行提交或简单的文件传输,然而这种形式的管理限制操作人员对试验进行实时的访问。可以实现机器可读格式临床数据互相操作性的eTMF新系统的出现则解决了这些局限,这不仅提高了药企对研发试验的审判效率还可以增进其与CRO企业间的沟通与协作。2015年5月,国家健康与护理卓越研究所(NICE)进行了一项医药外包服务公司的调查,该研究发现大约96%的药企偏好于与实施云技术(移动端和网络等技术)的CRO合作。
表4 云技术战略联盟


药物发现CRO服务涉及靶标确定、建立模型、先导药物发现及先导药物优化四大环节。CRO通过合同的形式向制药企业提供新药研发服务,涵盖新药研发的全过程或不同阶段,其根据覆盖的新药研发环节不同可分为药物发现、临床前和临床试验CRO。药物发现CRO主要负责提供靶点选择、新药发现、新药设计、药物筛选等工作。
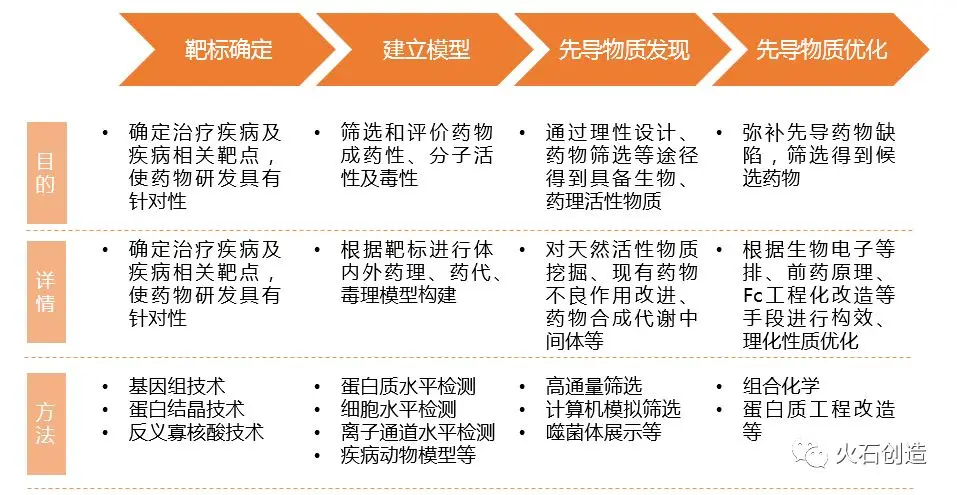
图1 药物发现CRO服务内容及环节
1.1 全球药物发现CRO市场规模达100亿美元,仅次于临床CRO
药物发现是新药创新的源头,在新药研发中具有举足轻重的地位。在新药研发愈发复杂、研发成本上升、专利悬崖多重压力下,更多的企业选择外包服务降低产品研发成本,提升研发效率。根据Frost &Sullivan数据显示,2013-2017年间,全球药物发现CRO年均复合增长率达9.5%,2017年全球市场规模达102亿美元(市场渗透率27.4%),仅次于临床研究CRO,占CRO服务市场总规模的22.9%。
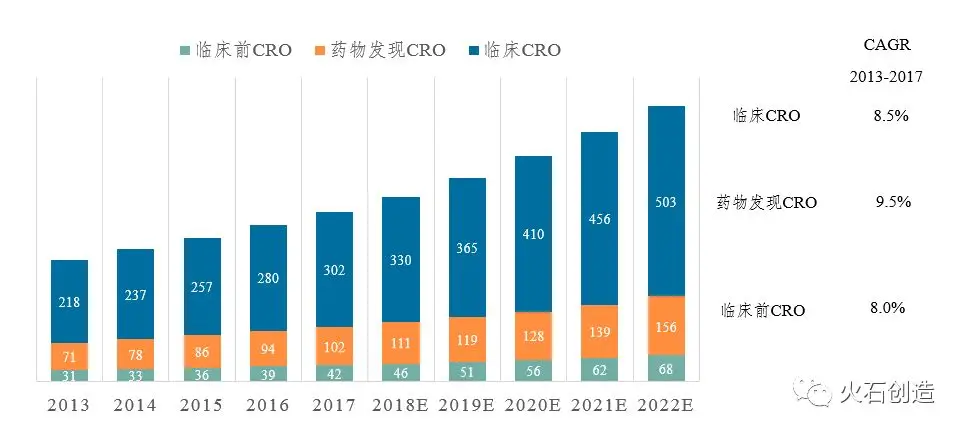
数据来源:Frost &Sullivan
1.2 全球药物发现服务市场较为分散,但市场集中度正在逐步提升
在药物发现CRO领域,查尔斯河实验室、药物康德、康龙化成、科文斯、昆泰IMS占据TOP5市场份额,2016年,这五家公司分别占据全球药物发现CRO服务市场的8.9%(查尔斯河收入包含药物发现和安全评价两部分)、3.0%、1.7%、1.5%、1.3%,TOP5公司市场集中度仅为16.4%,不过在2014-2016年间全球药物发现CRO市场集中度呈现逐年上升趋势。在药物发现阶段,由于研发成功率较低,出于谨慎考虑,药物研发企业倾向与规模化大型CRO企业进行合作,未来龙头企业的市场集中度有望进一步提升。
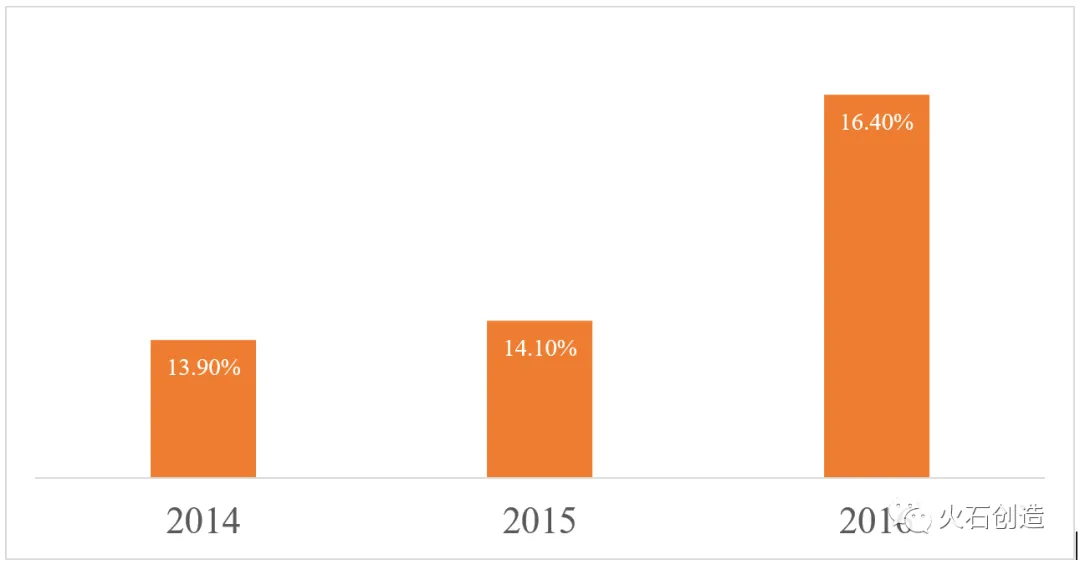
图3 全球TOP5药物发现CRO市场集中度
数据来源:Frost &Sullivan
2.1 我国药物发现CRO起步较晚,市场规模和渗透率有待提升
由于过去我国药品市场主要以仿制药为主,且企业的研发外包意识不强,中国药物发现CRO服务市场规模整体较小。Frost&Sullivan 数据显示,2017年,中国药物发现CRO服务市场规模仅1.4亿美元,渗透率仅13.2%,远低于全球水平的26.2%。不过近年来随着我国新药研发环境的逐步成熟,研发投入不断增加,我国药物发现CRO市场规模呈快速增长态势,2012-2017年年复合增长率达31.4%。
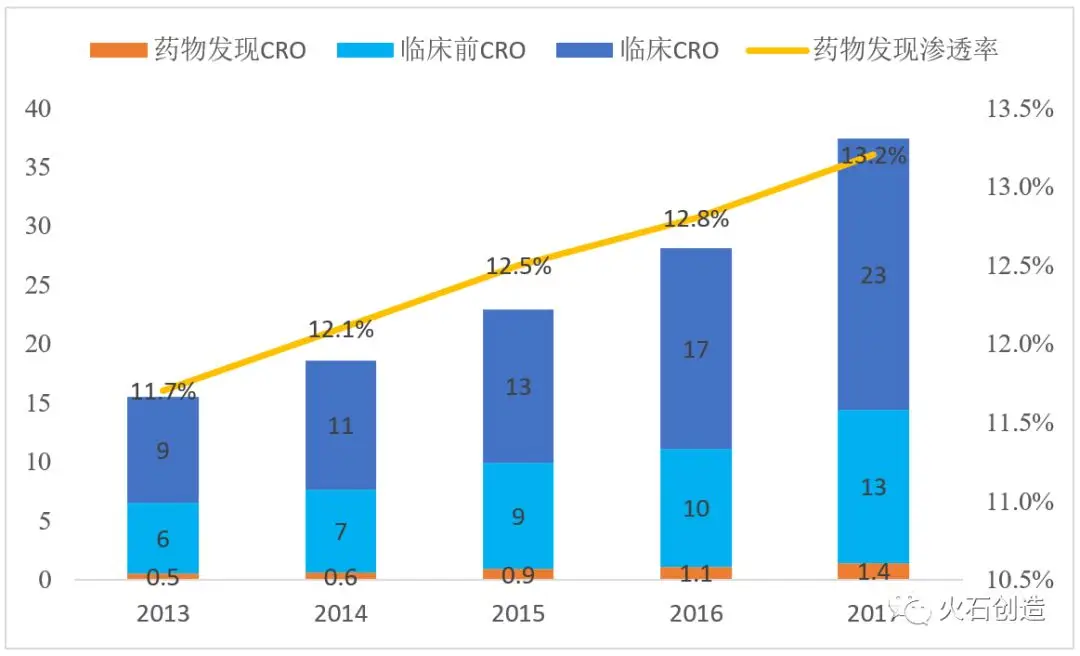
图4 中国CRO各细分领域市场规模
数据来源:Frost &Sullivan
2.2 国内药物发现CRO主要聚集在创新资源丰富的北上广苏地区
根据火石创造数据库统计显示,我国目前涉及药物发现服务的CRO企业有92家(包括药明康德等综合性CRO服务公司)。据企业的地域分布显示,涉及药物发现服务的CRO企业分布最多在北京(29家)、其次是上海(17家)、广东(14家)、江苏(12家)等新药研发企业密集分布区域。其中北京、上海地区借助丰富的产学研资源、人才资源及创新资源,汇聚了康龙化成、药明康德、睿智化学等药物发现龙头企业,及维亚生物、立迪生物、百奥赛图、保诺科技、益诺思、和铂医药、寻百会生物科技等中小型创新型企业。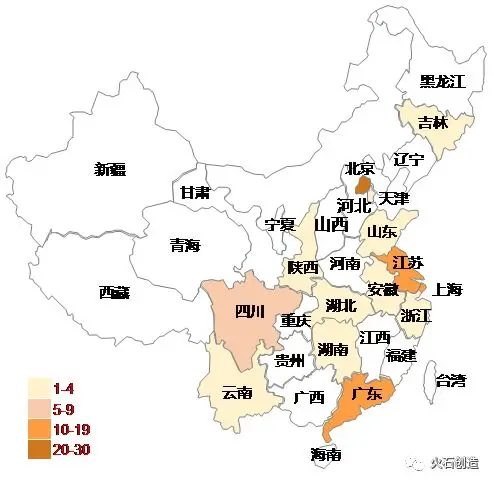
3.1 前瞻性药物发现CRO通过打造特色技术平台,提高新药发现效率构建行业竞争力
CRO行业产生的根本驱动力是为药企降低成本,因此对于药物发现CRO企业而言,通过创新性技术的使用,提升新药研发效率是构筑行业竞争力的有效手段。如维亚生物的基于ASMS筛选技术及多种化合物库的先导化合物发现引擎平台可实现6个月从筛选到共晶,1年到先导,3年到临床候选化合物的记录;药石科技构建的包含40000多种结构新颖、性能高效的药物分子砌块库,有助于帮助新药研发企业快速筛选到合适药物分子中间体;寻百会的CRISPR高通量筛选平台可用于新靶点、生物标记物及构建新型联合疗法研究,推进肿瘤治疗方法的研发速度和准度;成都先导的DNA编码化合物技术则具有合成分子数量大、速度快、成药性高的特点。
表1 国内药物发现CRO特色技术与服务(部分)

数据来源:公开资料整理
3.2 大型药物发现CRO与企业建立源头合作,提供药物研发一体化服务
大型药物发现CRO公司通过与客户在药物发现阶段进行源头合作,提供药物发现到临床前、临床研究,药物生产等一体化服务,使得客户对公司提供服务的需求随着新药开发过程的推进并最终商业化生产而不断增加,并使得公司来自每个项目的综合收益随着项目在新药开发周期中的推进而呈几何级数增加,这方面的代表公司有药明生物、康龙化成等。
四、小结
作为新药研发最前端的环节,药物发现在新药研发中具有举足轻重的地位。目前我国药物发现CRO市场整体市场规模仍较小,药物发现外包服务渗透率相比全球仍具有很大差距,市场规模及渗透率仍有较大的成长空间。从企业维度看,目前我国药物发现CRO企业全国约一百家左右,整体呈现龙头企业引领,中小企业创新特色发展局面,其中大型药物发现CRO通过与企业在药物发现阶段建立源头合作,提供药物发现一体化服务。中小CRO企业则通过特色技术平台或服务构建核心竞争力,在各个细分赛道领域实现突破。
近年来,随着政策改革、企业研发投入提高,我国临床CRO行业高速增长,2017年市场规模达 400 亿元。
一、临床CRO发展现状
1. 2017年全球临床CRO市场规模 302 亿美元,是CRO市场规模占比最大的子行业。
临床试验是新药研发中耗时最长、花费最高的环节,通常占据新药研发过程中 1/2 以上的费用和 2/3 的时间,专业的临床CRO公司可提供临床试验(I~IV期)患者招募与管理、临床监察、中心实验室、药物警戒、SMO、数据管理和分析统计等服务,提高制药企业新药上市的效率,逐渐成为医药研发产业链的重要角色。
目前全球约半数的制药企业通过CRO 开展Ⅰ~Ⅲ期药物临床试验,数据显示,2017年全球临床CRO市场规模达 302 亿美元,占CRO服务市场总规模的67.7%,是CRO市场占比最大的子行业。
注:2018—2022年为预测数据。
图1 全球CRO各细分领域市场规模
数据来源:Frost &Sullivan
2. 政策改革推动我国临床CRO行业高速增长,2017年市场规模约 400 亿元。
国内首家临床CRO是MDS于1996年在我国建立的分支机构,随着2003年我国颁布了《药物临床试验质量管理规范》明确规定申办者可以委托合同研究组织执行临床试验中的某些工作和任务,直接激活了临床CRO市场的迅速发展。
随着我国药品监管政策趋严,2015年后一系列医药改革政策促进国内企业研发投入,我国临床CRO市场规模随之水涨船高。数据显示,2013—2017年中国临床CRO市场年复合增速达24%,到2017年市场规模达 403 亿元。
3. 国内临床CRO企业“多强并举,两极分化”,呈金字塔分布。
凭借着低廉的人力和材料成本、庞大的患者人群和丰富的疾病谱,我国临床CRO行业迅速发展,但我国临床 CRO企业呈金字塔型分布,跨国 CRO企业和个别中国本土 CRO 凭借其强大的服务能力和品牌优势位于行业金字塔的顶端;数量迅速膨胀的国内中小型CRO 企业位于金字塔底部,相比国际巨头,其临床试验 CRO 的市场集中度较低,绝大多数企业服务内容单一,尚未形成规模化运营。
表1 国内临床CRO企业竞争格局
4. 国内临床CRO企业369家,主要分布在北上苏广等地。据火石研究院统计,目前国内涵盖临床CRO业务的医药外包企业共369家,主要分布在临床资源丰富及创新资源集聚的北京市、上海市、江苏省和广东省,其中聚集了众多优质临床医学学校及丰富临床经验的试验机构的北京成为了孕育临床CRO企业的摇篮。
截至2018年底,北京市具有临床CRO业务能力的医药外包企业数量高达144家,全国占比39.0%,并出现了一批在国内外具有一定影响力的专业临床CRO企业(不分先后),如诺思格、普瑞盛、永铭医学、赛德盛、万全阳光和海金格等。图3 中国临床CRO地域分布
1. 临床试验患者招募与管理流程有待完善。患者招募仍然会是未来几年临床开发的主要成本,虽然中国的患者池十分庞大,但目前国内临床试验在前期招募患者上极度缺乏经验以及完善的招募体系从而导致患者资源的浪费:(1)路径不通。由于信息不对称,大量病人均在无法进行临床试验的基层医院进行就诊治疗,如何打通路径,将病人引流入临床试验中是未来加速临床试验进展所必须解决的难题之一。
(2)难以精准匹配。目前国内对于患者的诊断数据收集较少,而诊断数据的有效分析将大幅提高临床试验开展的效率。在诊断过程中将符合条件的患者精准匹配至临床试验中,不仅能实现患者与试验方间的对接,也能在一定程度上提高临床试验的成功率。
2.临床试验设计与管理人才紧缺。临床试验CRO主要依靠专业技术人员提供服务,人才优势是其发展核心,优秀的临床试验设计和管理人才对于临床试验进度与质量起着至关重要的作用。以临床试验设计为例,默沙东K药凭借有效的试验设计将PD-L1表达水平作为患者入组限制要求而拉开与施贵宝O药在肺癌领域的差距,变身为肺癌领域适用最广的PD-1抗体药物。而在临床试验机构资源本就紧张的局面下,国内大量相同设计的临床试验涌现,这不仅降低了创新药的质量,还造成了患者资源和临床资源的过度消耗。相较国外已成熟的临床人才培养模式,国内几乎还处于空白期,尚未有高校设立如临床研究方法、医学统计、数据管理、伦理和医学项目管理等课程。3. 临床试验机构的量与质制约CRO服务水平。临床研究环节的瓶颈问题将成为影响中国药物研发进展速度的关键因素之一,国家及地方政府已在积极优化审批流程以解决此类问题。2018年11月,CDE官网增加了“临床试验默示许可公示”一栏,并公布了首批临床试验默示许可名单,中国正式进入了对新药临床试验默示许可的时代。但行政环节审批速度的加快也进一步对国内临床试验机构及人员资源提出了挑战。药物临床试验机构与PI的数量和质量直接决定了临床CRO研究的容量与服务水平。仅在2013—2018年期间,CDE共登记 7382 件临床试验。随着国内用药需求和研发热情的不断提高,临床试验的数目必然将维持高速增长的趋势,而这庞大的数字对国内在临床方面上的稀缺资源——临床试验机构及PI而言均是一项非常艰巨的任务。
1. 临床CRO业务趋于全球化。2017年6月,CFDA正式成为国际人用药品注册技术协调组织(ICH)全球第8个监管机构成员,通过与国际标准和指南同步,国内临床试验的质量与标准将与国际接轨,通过标准的提升促进国内本土制药企业加强创新能力和国际竞争力。国内 CRO 可通过加强与国外 CRO 合作,学习先进的运作和管理经验;国外 CRO 也可以为本土 CRO 的发展提供更多的人才, 但同时必然与国内 CRO 形成有力竞争。2. 龙头企业横向拓展,中小企业精细化发展。CRO龙头在发展主营CRO 业务的同时,临床CRO也在不断探索可持续发展的新型业务模式。如泰格医药公司近年来参与设立多支医药产业投资基金和并购基金,先后成立杭州泰格股权投资、TG Sky investment作为公司境内、境外投资平台进行专业化投资,致力于发掘和培育境内外优质的创新型医药企业,一方面获取投资收益,另一方面帮助公司业务范围和规模。中小企业受制于资金、管理等原因,形成综合性业务能力突出的 CRO 公司需要发展时间,业务精细化发展是其发展的方向之一,形成了分别专注于上市后再评价、仿制药一致性评价、Ⅰ期临床试验、真实世界研究和SMO业务等领域的 CRO。3. 临床CRO临床试验数据管理逐步信息化。合同研究具有信息密集的特点,近年来越来越多的CRO正在加大大数据利用技术方面的投资,提高自身的数据管理能力,这其中最具代表性的就是临床试验数据的管理。临床实验数据采集和管理会直接影响药物研发临床试验的质量。信息化水平的提升可以有效减少药物研发的时间,缩短新药上市的流程,目前多数CRO企业使用的是TMF(TrialMaster File)模式对临床试验数据进行管理,即使用纸质形式对临床数据进行提交或简单的文件传输,限制了操作人员对试验进行实时的访问。近年来,CRO逐步由传统的纸质化的临床数据采集和数据管理模式转向电子化的临床数据采集和数据管理。这不仅提高了药企对研发试验的审判效率还可以增进其与CRO企业间的沟通与协作。此外,随大数据、物联网及智能可穿戴设备的发展,临床CRO企业开始尝试通过可穿戴设备、医疗器械装备等进行患者招募、远程收集参与者的临床数据、活动数据和关键的生物指标,减少随访及跟踪次数,结合电子化的临床数据采集和数据管理可大大而提升效率,降低临床试验成本。
四、小结
近年来,随着政策改革、企业研发投入提高,我国临床CRO行业高速增长,2017年市场规模达 400 亿元。
作为CRO业务中占比最大的子行业,国内临床CRO行业快速发展的同时面临临床试验患者招募与管理流程有待优化、临床试验设计与管理人才紧缺、创新药物快速发展对临床试验机构及人员资源提出更高要求等挑战。
未来随着我国加入ICH,临床CRO和数据行业融合等,我国临床CRO企业业务将呈现业务全球化、服务创新化、管理信息化等趋势。
